-
.Grazie della spiegazione Ramirez, confermi quello che immaginavo. Cioè che sul totale delle forze che creano un impasto questo fenomeno non è preponderante
Purtroppo l'ossidazione dell'impasto è diventata una fissa ......nascono quindi le più svariate teorie come questa dell'ossigenazione mediante pieghe che è riportata in diversi forum.. -
....
La formazione della macromolecola glutine oltre che dalla presenza dell'acqua è determinata dalla energia meccanica impartita durante la miscelazione e l'impastamento, questa energia meccanica induce cambiamenti conformazionali delle proteine del grano, vale a dire, la rottura e la formazione di entrambi i legami sia covalenti (-SS-) che non covalenti (idrofobico e idrogeno) (Aït Kaddour e altri 2008). La presenza dell'ossigeno migliora la struttura favorendo la formazione dei ponti disolfuro intra e intermolecolari . Ma comunque i legami covalenti a ponte disolfuro si formano come detto anche dalla sola energia meccanica impartita per la formazione dell'impasto e questo spiega la funzione delle pieghe .
....
Però! Ora sì che tutto è più chiaro.
Davvero grazie
Ancora una curiosità: i legami ionici invece sono quelli del sale? Quindi troppo sale, più legami, maggior/troppa forza.... -
.Ma comunque i legami covalenti a ponte disolfuro si formano come detto anche dalla sola energia meccanica impartita per la formazione dell'impasto e questo spiega la funzione delle pieghe .
Non ho capito se parli degli entanglements. -
.
1-Si , i sali inducono rigidità alla macromolecola , infatti quando aggiungi sale l'impasto prende corda.
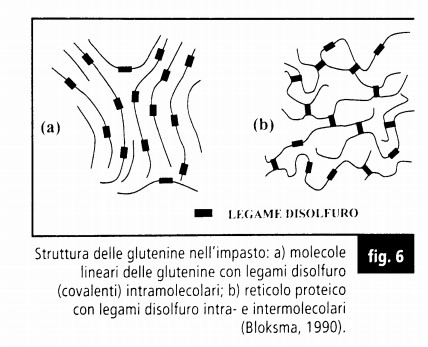
2-Mi riferisco ai legami a ponte disolfuro che vengono facilitati dalla forza meccanica impressa all'impasto ,ciooè due catene polimeriche vengono avvicinate dalla forza meccanica e vengono favoriti in tal caso i legami a ponte disolfuro.
Edited by ramirez - 12/3/2017, 23:14. -
.
I legami disolfuro avvengono per ossidazione dei gruppi tiolici della cisteina. L'ossidazione avviene grazie ad un elemento che si riduce che può essere l'ossigeno. Può avvenire anche grazie ad altri elementi.
Ramirez, quando parli di legami disolfuro che avvengono per l'azione meccanica anche senza ossigeno intendi che la farina ingloba già altri ossidanti?
Mi chiedo, cioè, che percentuale approssimativa di legami disolfuro è dovuta all'ossigeno inglobato e quale all'azione meccanica?
Sto cercando di capire quindi l'importanza di inglobare ossigeno. E' questo l'ossigeno che partecipa alla redox?
Infine (purtroppo i dubbi che vorrei chiarire sono molti...) l'O2 è sempre in quantità sufficiente? E' possibile che in questa fase lo si usi tutto. Immagino di sì visto che si aggiunge acido ascorbico in casi di poco ossigeno per dare forza alla farina.
Mi interessa perché l'ossigeno serve anche ai lieviti per moltiplicarsi... e quindi questi ragionamenti possono essere collegati
tutto si sta chiarendo ma ho bisogno ancora di un "piccolo" aiuto😋
ti ringrazio
marco
Edited by balos - 13/3/2017, 15:59. -
.
balos
La risposta te l'avevo data più sopra in un commento , quando ho detto che ci sono altre molecole che funzionano da ossidanti e che quindi favoriscono la formazione di legami a ponte disolfuro. Anzi c'è un meccanismo molto complesso che non mi dilungo a spiegare.
Questa dell'ossigeno è una fissa!!!! contribuisce ma non è determinante , in tanti hanno questa preoccupazione ma non ha ragione di esistere .
La manipolazione dell'impasto come ho detto stira i polimeri e li avvicina e quindi è più facile per sostanze ossidanti come la PDI e GSH ossidare nuovi legami , ci saranno anche meccanismi come l'entanglement a formare legami fisici.
L'ossigeno è sempre sufficiente anche per la lievitazione aerobica.. -
.
Hai ragione, non avevo colto!
grazie mille
Marco. -
.balos
La manipolazione dell'impasto come ho detto stira i polimeri e li avvicina e quindi è più facile per sostanze ossidanti come la PDI e GSH ossidare nuovi legami
Mi sa che sono una capra!




Ho bisogno di una dose di VOLPAZIN...
Penso di aver capito e poi leggo qualcosa e mi accorgo che sono nuovamente in alto mare.
Ramirez, non voglio monopolizzare il tuo tempo, magari se anche qualcun altro interviene sarebbe un aiuto. Anzi ti ringrazio nuovamente per la pazienza.
Parliamo del glutatione (GSH). Leggo che è un antiossidante e quindi immagino che non faccia avvenire l'ossidazione dei gruppi tiolici della cisteina ossidandosi lui stesso. Immagino quindi che limiti la formazione dei legami disolfurici e determini un impasto più facilmente estensibile.
Ho letto poi che una volta ossidato è in grado, con un certo procedimento, di tornare alla forma ridotta pronto nuovamente ad ossidarsi.
Quanto riporti sopra invece dice esattamente il contrario!!!!
E io torno in alto mare...

va là, ora mi iscrivo alla convection... temete!. -
.
Discussione molto interessante. Un aspetto che mi ha incuriosito nel tempo è la composizione delle farine di forza dove ora prevalgono le glutenine, ora le gliadine. Come riconoscerle e come poterle lo stesso impiegare, magari correggendo le procedure. . -
.Discussione molto interessante. Un aspetto che mi ha incuriosito nel tempo è la composizione delle farine di forza dove ora prevalgono le glutenine, ora le gliadine. Come riconoscerle e come poterle lo stesso impiegare, magari correggendo le procedure.
vediamo... a parità di W (lavoro) maggiore è il rapporto P/L e maggiore è la tenacità che è legata alla presenza di più glutenine rispetto alla farina con P/L inferiore.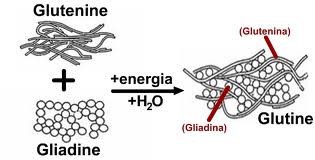
Edited by balos - 14/3/2017, 21:40. -
.
balos
Il GSH è una molecola che ha un doppio comportamento come la PDI , in forma ossidata funziona da ossidante , ma è un discorso lungo e ancora non ben chiarito sarebbe quindi non mi dilungo.. -
.Discussione molto interessante. Un aspetto che mi ha incuriosito nel tempo è la composizione delle farine di forza dove ora prevalgono le glutenine, ora le gliadine. Come riconoscerle e come poterle lo stesso impiegare, magari correggendo le procedure.
vediamo... a parità di W (lavoro) maggiore è il rapporto P/L e maggiore è la tenacità che è legata alla presenza di più glutenine rispetto alla farina con P/L inferiore.

Non è solo la quantità di glutenine a rendere elastico e tenace l'impasto , ma anche la complessità di legami intra e inter molecolari a ponte disolfuro.
A complicare poi il P/L interviene anche l'assorbimento e qui il discorso è un po più complesso.. -
.Scusate, una domanda semplice. Cos'è che conferisce gommosità, specie quando la pizza si raffredda?
Copio incollo
Da quello che ho potuto desumere, a quanto pare le cause della gommosità possono essere due:
1) RETICOLO PROTEICO ECCESSIVAMENTE NERVOSO: pare che il prodotto finale risulti gommoso quando l'impasto ha un reticolo proteico troppo rigido (per esempio la maglia glutinica - vuoi perchè l'impasto non ha riposato a dovere, vuoi perchè l'impasto era troppo freddo - non ha ricevuto ora i tempi ora le condizioni ambientali favorevoli per il suo rilassamento);
2) ECCESIVA FERMENTAZIONE/ACIDITÀ DELL'IMPASTO: pare che una fermentazione protratta oltre il dovuto rilasci all'interno dell'impasto delle sostanze (soprattutto l'acido acetico) che in cottura restituiscono gommosità al prodotto finale.
magari apri un thread che ne parliamo
ciao
Marco. -
ibinsad.
User deleted
Ma perché per dare forza all'impasto si aggiungerebbe la vitamina c, non ho ben capito che reazioni genera.
E che differenza ci sarebbe tra aggiunta di vitamina c o del glutine secco per dare forza?. -
.
se ben mi ricordo, la vitamina c o acido ascorbico aiuta a far creare i ponti disolfuro, praticamente fa creare più legami al glutine, quindi rende più forte una farina "debole" alzando anche di 40 o 50 punti il W della farina.
di contro ti rende più rigida la maglia e se devi fare pizza, ti rende più difficile la stesura.
con il glutine secco altro non fai che aumentare la quantità di glutine all'interno della farina.
L'OSSIDAZIONE DELL'IMPASTO |
